我們開發了一種專有的技術平臺,能夠快速降解免疫球蛋白G(IgG)。該平臺采用全球領先的低預存抗體IgG降解酶,通過靜脈給藥,能迅速且完全清除血漿和組織中的總體IgG。
IgG是人體血清中免疫球蛋白的主要成分,約占血清總蛋白總含量的10-20%。正常情況下,IgG能夠保護人體免受外來病原的傷害。然而,在某些疾病狀態下,如IgG型多發性骨髓瘤或由致病性IgG引起的自身免疫性疾病(如腎小球基底膜病、格林-巴利綜合征、重癥肌無力等),IgG是致病因素。
正常IgG也可能阻礙一些患者生命攸關的急性治療需求。在異體或異種器官移植中,人體內的IgG會識別供體組織中的非自身抗原,激活免疫系統,導致排斥反應。在以病毒載體為基礎的基因治療中,IgG可能會中和載體使之無效。
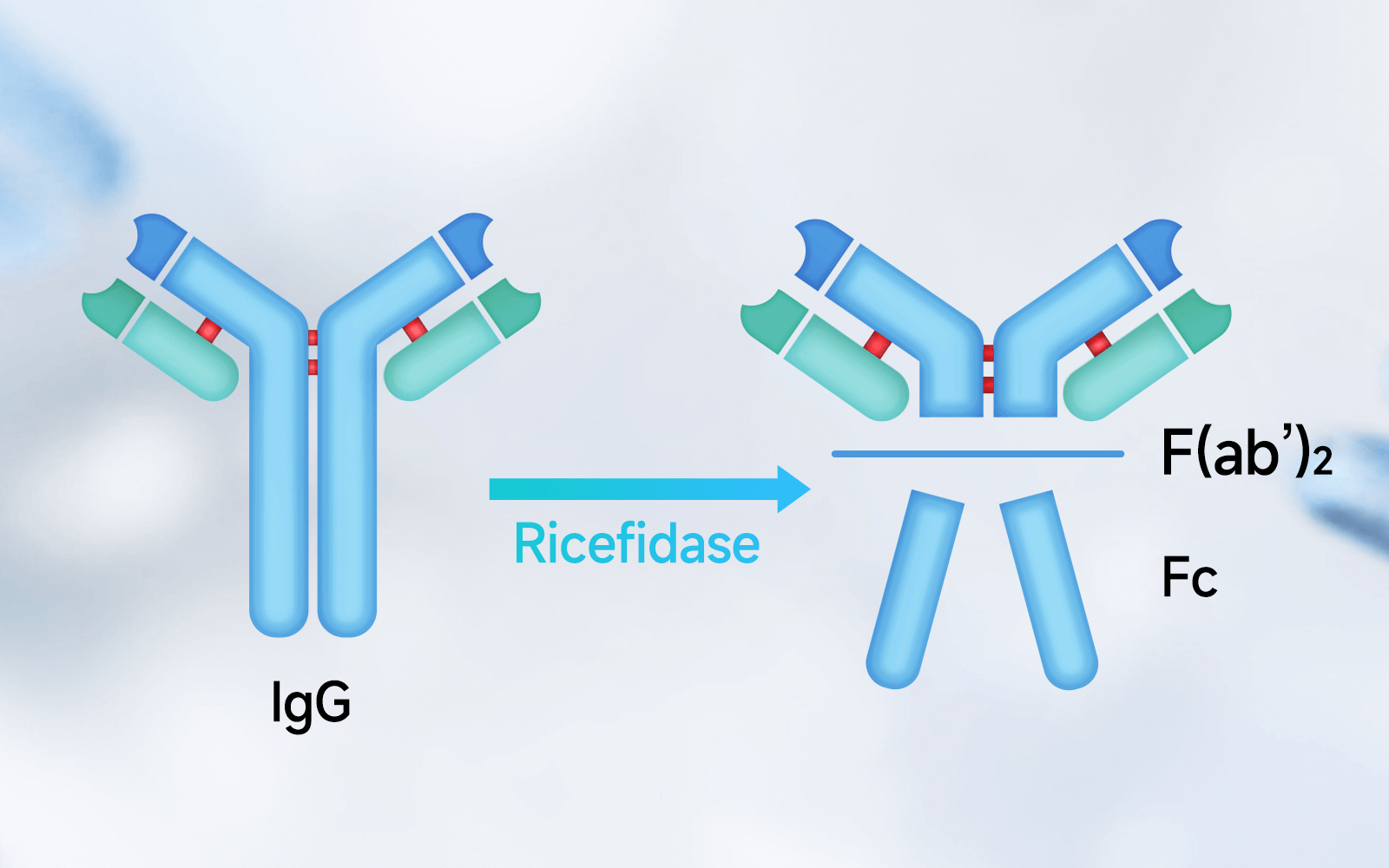
針對如此量級的致病或幹擾治療的IgG,常規醫療管理手段生效慢且昂貴。Ricefidase是全球領先的新一代IgG降解酶,它來源於不感染人類的化膿性鏈球菌的酶,通過我們自主研發設計改構而獲得。Ricefidase能夠高度特異性地降解IgG的下鉸鏈區,使其失活。
在新西蘭和中國完成的I期臨床試驗已經證明,在給予Ricefidase後的1到2小時,受試者血清和組織中的IgG幾乎全部被酶切清除。被酶切後的片段無法介導依賴Fc的病理機製,從而防止和抑製不良免疫反應,如依賴IgG的補體激活、細胞殺傷和細胞活化等。
與人體內預存抗體高達85%以上、在歐洲獲批上市的伊立菲酶相比,Ricefidase在人體內的預存抗體比例低於20%,且具有低免疫原性,因此可以與免疫抑製劑如MTX聯合使用。Ricefidase還能用於增加治療窗口期,具備更廣泛的適應癥潛力,例如需要重復給藥的自身免疫性疾病治療,致敏性器官移植後的維持治療、基因治療以及IgG型多發性骨髓瘤等腫瘤治療。
2022年03月Ricefidase獲新西蘭藥監(Medsafe)批準開展I期臨床試驗。
2022年05月Ricefidase獲FDA臨床試驗許可,用於治療一大類由病理性IgG導緻的自身免疫性疾病。
2022年08月Ricefidase獲NMPA臨床試驗許可,用於高度緻敏的腎移植患者脫敏治療。
2023年04月Ricefidase在中國、新西蘭分別完成I期臨床試驗(CTR20222595/NCT05274659)。
2024年08月Ricefidase獲NMPA臨床試驗許可,用於抗GBM病治療。
2024年11月Ricefidase在高度緻敏的腎移植患者脫敏治療被NMPA納入“突破性治療品種名單”。
2024年12月Ricefidase在中國完成高度緻敏的腎移植患者脫敏治療II期臨床試驗(CTR20234137)。
2025年04月Ricefidase獲NMPA臨床試驗許可,用於GBS病治療。
2025年07月Ricefidase用於抗GBM病治療被NMPA納入“突破性治療品種名單”。
2025年08月Ricefidase在中國啟動用於高度緻敏的腎移植患者脫敏治療III期臨床試驗(CTR20252973)。
2025年10月Ricefidase在中國完成抗GBM病II期臨床試驗(NCT06607016)。
2025年11月Ricefidase在中國啟動GBS病II期臨床試驗(CTR20253992)。
2025年11月Ricefidase在中國開始籌備GBM病III期臨床試驗。

我們的生產過程符合現行GMP要求,臨床期間的生產規模滿足未來商業化的需求。